从单枪匹马到同舟共济:头颈鳞癌免疫治疗进阶之路
发表时间:2018-11-03 09:02:00
头颈鳞状细胞癌(HNSCC)是常见的恶性肿瘤之一,每年新发病例超过55万,死亡病例达38万。常见的头颈部鳞癌包括:鼻腔鼻窦癌、口腔癌、扁桃体癌、咽喉癌等恶性肿瘤。吸烟和酗酒为HNSCC的常见因素,人乳头瘤病毒(HPV)感染也与口咽癌发病密切相关。
大多数局部晚期HNSCC患者通常接受手术、放疗和全身治疗。然而,近年来,随着手术和放疗技术发展,化疗和EGFR靶向单抗治疗被纳入局部晚期HNSCC治疗,但是超过一半的患者最终却发生了复发或远处转移。即使应用现代多药物化疗,不可治愈或转移性复发患者的中位生存期仍低于1年。免疫治疗的出现无疑为抗癌治疗提供了强有力的支撑。
目前已有多个临床研究评估了免疫检查点抑制剂单药或联合治疗在HNSCC中的应用。帕博利珠单抗和纳武利尤单抗已经获批用于复发/转移 HNSCC的二线治疗,但是并非所有的患者都对此有反应。Durvalumab,一种阻断PD-L1与T细胞上的PD-1和CD80结合的人源单克隆抗体,在复发/转移 HNSCC中也显示出作为单一疗法的抗肿瘤活性。
由于肿瘤免疫的过程复杂,多种机制的共同作用影响了免疫检查点抑制剂的疗效,单药治疗的反应率还有很大提升空间。而免疫联合疗法可以进一步提高患者对肿瘤免疫药物的适用率和受益率、减少反应时间、增强对肿瘤症状/进展的临床控制、延长患者对药物反应的程度和持续时间。基于现有肿瘤免疫治疗的现状,在研究者们的努力下,更优化的免疫治疗方案不断涌现,免疫治疗正在进入2.0时代。
KEYNOTE-048研究
复发/转移头颈部鳞癌的一线标准治疗方案为EXTREME方案(西妥昔单抗联合含有顺铂或卡铂的5-氟尿嘧啶)。KEYNOTE-048是一项关于一线应用帕博利珠单抗单药或联合化疗,对比EXTREME方案治疗复发/转移头颈部鳞癌的开放的随机3期临床试验。该研究结果于今年ESMO大会重磅发布。
研究方法
KEYNOTE-048研究共入组882例患者,1:1:1随机分配到帕博利珠单抗单药组(P组,帕博利珠单抗200mg Q3W,共35周期),帕博利珠单抗联合化疗组(P+C组,帕博利珠单抗200mg Q3W,共35周期),联合卡铂AUC 5 或顺铂100mg/㎡加5-FU 1000mg/㎡/d 连续4天给药,6个周期(每3周),或者EXTREME组(E组),西妥昔单抗250mg/㎡Q1W,联合卡铂AUC 5 或顺铂100mg/㎡加5-FU 1000mg/㎡/d 连续4天给药,6个周期(每3周)。
给药至疾病进展或毒性不可耐受。主要研究终点为在PD-L1综合阳性评分(CPS)≥20,CPS≥1和所有阳性患者中,分别比较P组,P+C组对比E组的PFS和OS。
研究结果
?P组 vs E组
在PD-L1 CPS≥20和CPS≥1的患者P组的OS优于E组(N = 255; 中位14.9 vs 10.7 个月; HR 0.61 [95% CI 0.45-0.83]; P = 0.0007;N = 512; 中位12.3 vs 10.3 个月; HR 0.78 [95% CI 0.64-0.96]; P = 0.0086)。在总人群中,P组的OS不劣于E组。
在PD-L1 CPS ≥20和CPS≥1的患者P组和E组PFS无显著差异(mPFS3.4 vs 5.0个月;HR 0.99, 95%CI 0.75-1.29;mPFS3.2 vs 5.0个月;HR 1.16, 95%CI 0.96-1.39)。
在PD-L1 CPS≥20的患者中,P组和E组的ORR分别为23.3% vs 36.1%,中位DOR分别为20.9 vs 4.2个月。在PD-L1 CPS≥1的患者中,P组和E组的ORR分别为19.1% vs 34.9%,中位DOR为分别为20.9 vs 4.5 月。在总人群中,P组和E组的ORR分别为17% vs 36%,中位DOR为分别为20.9 vs 4.5 月。
安全性分析:总体人群中,P组和E组治疗相关的不良事件(AEs)对比显示,帕博利珠单抗的耐受性更好。任意级别TRAEs发生率,两组分别为58.3% vs 96.9%;3-5级TRAEs发生率分别为16.7% vs 69.0%;两组分别有4.7%和19.9%的患者因为AE导致治疗中断。总体人群中,免疫介导的AEs对比,P组稍高。P组和E组任意级别的免疫相关AEs发生率分别为30.3% vs 23.7%;3-5级AE发生率分别为6.7% vs 10.5%。
?P+C组 vs E组
在总人群中,P + C组OS优于E组(N = 559; 中位13.0 vs 10.7 个月; HR 0.77 [95% CI 0.63-0.93]; P = 0.0034)。但两组的PFS对比无差异(mPFS分别为4.9 vs 5.1个月;HR 0.92;95%CI 0.77-1.10,P=0.2)。ORR对比,两组也无显著差异,分别为35.6% vs 36.3%,但P + C组的DOR更长,分别为6.7 vs 4.3个月。
安全性对比,P+C组与E组安全性相似,任意级别TRAEs发生率,两组分别为95.3% vs 96.9%;3-5级TRAEs发生率分别为71.0% vs 69.0%;因TRAEs导致治疗中止的患者比例分别为22.8% vs 19.9%。任意级别免疫相关AEs和输液反应的发生率,两组相当,分别为25.7% vs 23.7%。3-5级免疫相关AEs和输液反应的发生率,帕博利珠单抗联合化疗组更低,分别为4.7% vs 10.5%。
研究结论
相较于标准疗法,帕博利珠单抗一线治疗复发/转移性头颈部鳞癌患者在单药治疗PD-L1 CPS ≥20 和≥1的人群以及联合化疗的总人群中观察到了生存获益。这些结果为帕博利珠单抗和帕博利珠单抗+铂+5-FU作为治疗复发/转移头颈部鳞癌的一线标准治疗方案提供了数据支持。该研究将会继续以便获得最终的OS结果。
CONDOR研究
双靶向免疫疗法是一种可以提高单药治疗效果的方法,并且PD-L1单抗结合CTLA-4单抗显示出增强的临床前和临床抗肿瘤活性。此外,PD-L1抗体durvalumab联合CTLA4 抗体tremelimumab,在PD-L1低表达/阴性肿瘤患者中具有特异性疗效。
11月1日,JAMA Oncology 杂志在线发表了2期临床试验CONDOR的积极结果。这是第一个在PD-L1低表达或阴性(TC <25%)复发/转移性头颈部鳞癌患者中使用durvalumab单一疗法进行的研究。
研究方法
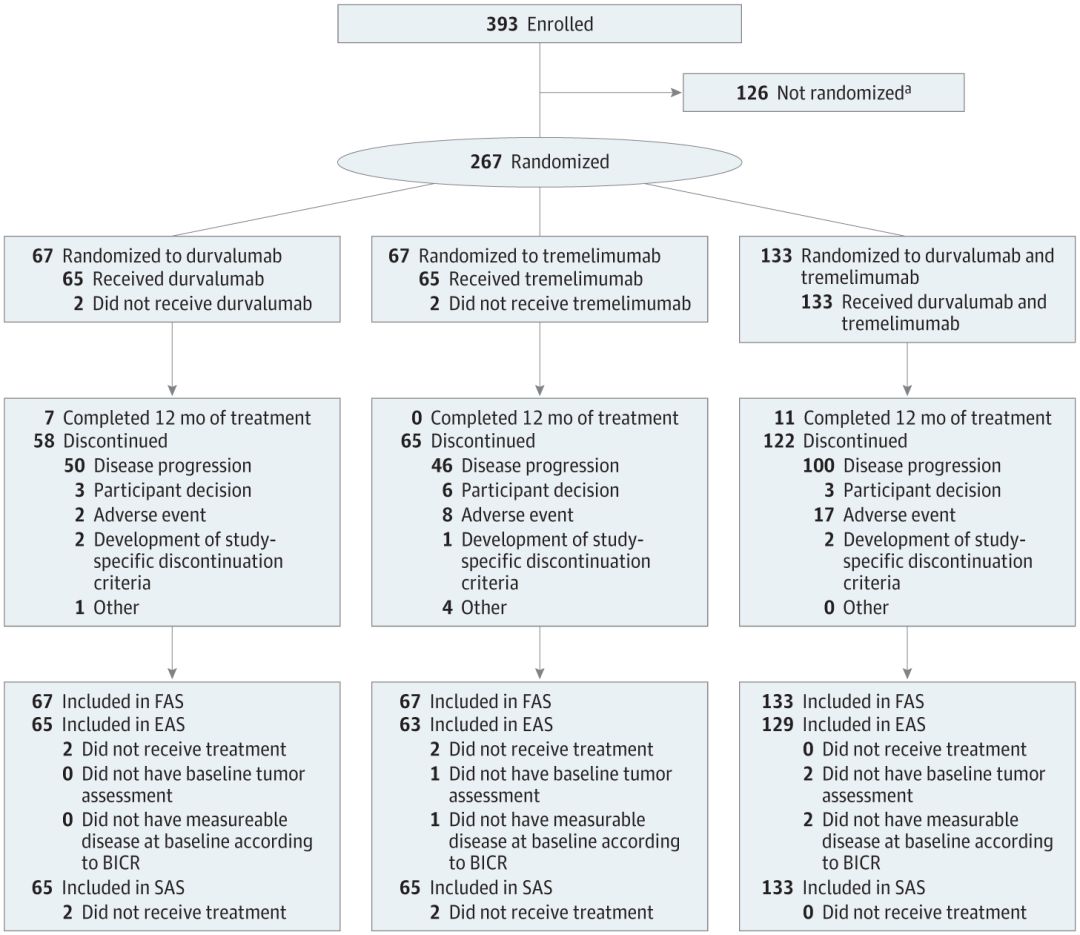
研究共入组了267例转移性(64%)或复发性(36%)的口腔癌,口咽癌,喉咽癌或喉癌患者,这些患者对既往含铂类化疗无效,且PD-L1低表达或阴性。
根据HPV状态和吸烟状况对患者进行分层,然后以2:1:1随机分为三个治疗组:单独使用durvalumab(10mg / kg,IV Q2W)(67例),单用tremelimumab(10mg / kg IV Q4W×7,然后Q12W×2)(67名患者),或durvalumab加tremelimumab(20mg / kg D Q4W + 1毫克每公斤 T Q4W×4,然后10mg / kg D Q2W)(133名患者)。主要研究终点为客观反应率(ORR)。
研究结果
研究显示,durvalumab单独或联合tremelimumab显示出令人鼓舞的抗肿瘤活性。在267例患者中(220例男性[82.4%]),患者的中位年龄为61.0[23-82]岁。),durvalumab单药组(n = 65)的ORR为9.2%,durvalumab + tremelimumab组(n = 129)为7.8%,tremelimumab单药组(n = 63)为1.6%。Durvalumab的ORR与其他PD-1/PD-L1抑制剂一致。
durvalumab + tremelimumab中位总生存期为7.6个月,durvalumab为6.0个月,tremelimumab为5.5个月。单用durvalumab和durvalumab联合tremelimumab的临床活性没有观察到差异。

durvalumab + tremelimumab治疗的21例患者(15.8%)发生3/4级治疗相关不良事件,durvalumab治疗组8例(12.3%),tremelimumab治疗组11例(16.9%)。仅在联合治疗组中8名患者(6.0%)发生3/4级免疫介导的不良事件。
研究结论
在PD-L1低表达或阴性的复发/转移性头颈部鳞癌患者中,durvalumab和durvalumab + tremelimumab两种方案具有临床获益,两者之间观察到的差异很小。3种方案均表现出可控的不良反应。第3阶段的研究正在进行中。
除此之外,在晚期或转移性头颈部鳞癌患者观察nivolumab与ipilimumab联合一线应用对比EXTREME方案疗效的III期临床试验CheckMate 651也正在进行中。我们期待更多的研究成果为头颈鳞癌患者提供最佳的治疗选择。目前对于免疫联合治疗还有很多问题需要明确,需要在具体临床实践中权衡有效性和安全性,从而选择最佳的肿瘤的治疗模式。
文章来源网络,如有侵权,请联系删除。