溶瘤病毒竟可杀伤肿瘤细胞,以毒攻毒的法子竟真有用?
溶瘤病毒是一类具有复制能力的肿瘤杀伤型病毒,世界上出现溶瘤病毒的报道,是由于1912年的意大利一位宫颈癌患者感染狂犬病毒后,肿瘤随之消退。
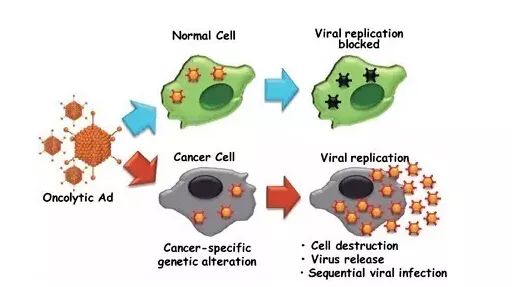
溶瘤病毒代表了一类新的治疗剂,它通过依赖于选择性肿瘤细胞杀伤和全身抗肿瘤免疫诱导的双重作用机制来促进抗肿瘤反应。目前溶瘤病毒(OVs)治疗癌症正处于快速发展阶段。
一项随机III期临床试验表明,接受改良单纯疱疹病毒1型(HSV-1)治疗的晚期黑色素瘤患者的持久缓解率有所提高,该病毒编码粒细胞-巨噬细胞集落刺激因子(GM-CSF)。这种病毒被称为talimogene laherparepvec(T-VEC),T-VEC是美国食品药品监督管理局(FDA)批准用于治疗初始手术后不可切除的黑色素瘤复发的溶瘤病毒。在肿瘤内给予T-VEC免疫疗法时,它会导致直接肿瘤细胞死亡并作为抗原的来源,有利于免疫细胞局部募集到肿瘤微环境中。T-VEC通过细胞表面的疱疹病毒糖蛋白进入癌细胞,有利于复制并最终引发细胞裂解。通过这种方式,肿瘤源性抗原(TDA)、GM-CSF和新的病毒颗粒被释放出来,从而一次性感染周围的肿瘤细胞并增强TDA的扩散,然后与危险相关的分子通路被激活,引起全身抗肿瘤作用和完全免疫反应。
T-VEC作为局部免疫疗法可杀死皮肤和淋巴结中的黑色素瘤细胞。一项关于T-VEC对50名局部晚期或转移性黑色素瘤患者进行的单臂 II 期研究结果显示,总缓解率(ORR)为26%,其中8例完全缓解(CR)和5例部分缓解(PR)。据报道,注射性和非注射性病变(包括内脏病变)的肿瘤负荷缩小,大多数反应(92%)维持近3年。12个月和24个月的总生存率(OS)分别为58%和52%。
一位62岁患者在出现2个巨大的踝骨病变和肢端黑色素瘤的淋巴结转移后接受了为期2年的T-VEC治疗,实现了完全缓解,治疗结束后持续2年。
但是T-VEC在一些患者的临床试验中的疗效有限,所以寻找加强溶瘤病毒治疗的新型溶瘤病毒是很有必要的。
近日,一篇题为“The potential of swine pseudorabies virus attenuated vaccine for oncolytic therapy against malignant tumors”的文章表明减毒猪伪狂犬病毒(PRV-LAV)是治疗NRP1/EGFR通路相关肿瘤的重要潜在候选药物。该研究为探究PRV-LAV的治疗效果,通过皮下注射多形性胶质母细胞瘤(GBM)细胞、HepG2细胞或A549细胞到雌性BALB/c裸小鼠体内,建立肿瘤异种移植小鼠模型。肿瘤病变生长到约100 mm3的体积,然后用PRV-LAV或对照治疗小鼠。研究发现用HepG2和GBM细胞在裸鼠体内建立的肿瘤在PRV-LAV治疗后被完全清除,并且在较长时间内没有复发。同样,用PRV-LAV处理裸鼠A549细胞形成的肿瘤也明显受到抑制。
另外在探索PRV-LAV作用的免疫机制研究中发现免疫抑制分子PD1和TIM3的表达降低,同时PRV-LAV处理后活化CD8 T细胞中与T细胞毒性活性相关的颗粒酶B的表达增加。这些发现表明,肿瘤浸润性CD8T细胞比例的增加可能会将肿瘤环境从免疫抑制状态转变为免疫刺激状态。在耗尽的CD8T细胞、na?ve中性粒细胞和活化的中性粒细胞中,颗粒酶B的表达也增加。
总而言之PRV-LAV可以通过激活CD8T细胞的抗肿瘤功能发挥抗肿瘤活性。而溶瘤PRV-LAV或将将成为人类肿瘤治疗武器库中的重要工具。
文章摘自网络,侵删
同类文章排行
- 溶瘤病毒竟可杀伤肿瘤细胞,以毒攻毒的法子竟真有用?
- 室管膜瘤什么病?室管膜瘤有哪些类型?
- 29岁姑娘无症状确诊肺癌,医生提醒:这几种肺结节要警惕!
- 横扫多类癌种!WT1树突状细胞疫苗实现抗癌新突破
- 康铁邦、廖丹、钟理团队揭示骨肉瘤中的抑癌基因L3MBTL2及其调控机制
- 张进团队开发第二代iPS来源的CAR-巨噬细胞,在细胞治疗实体瘤领域取得系列突破
- 放化疗后肿瘤仍复发?联合细胞治疗复发更少,5年生存率超88%
- 华人学者研究发现:只喝酒不吃饭,胃肠道癌症风险增一半
- 现如今癌症发病率如此高,我们要如何预防呢?
- 血液肿瘤克星“CAR-T细胞疗法”的疗效受到哪些因素的影响?
最新资讯文章
您的浏览历史








