NGS助力甲状腺癌患者检出RET融合,多角度指导临床诊治!
甲状腺结节已经是常见病。由中华医学会内分泌学分会领衔发布的《甲状腺结节和分化型甲状腺癌诊治指南(第二版)》明确提到,20.43%(约1/5)的中国成人通过超声检查存在直径0.5cm以上甲状腺结节,且展现出逐年上升的趋势,其中8%—16%为的结节恶性肿瘤,而甲状腺结节评估的主要目的是鉴别其良恶性。共识这里引用的数据正是由中国医科大学第一医院等30多家医院共同发表在Thyroid期刊上的TIDE研究,该研究覆盖了中国大陆31个省的甲状腺结节人群数据,具有极高的代表性。现阶段,随着甲状腺癌分子机制的研究深入,涌现出BRAF、RET、SPOP等多个基因,能够为甲状腺结节的良恶性鉴别及用药指导提供依据。
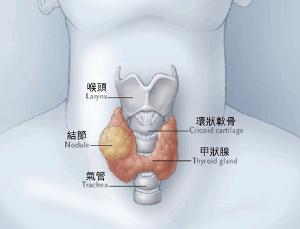
图片来源于网络,侵删
近期,我司为一位甲状腺乳头状癌(PTC)患者检出CCDC6-RET融合,从不同角度为患者提供了临床诊疗和管理。
案 例
患者信息:女、43岁
临床诊断:乳头状甲状腺癌(PTC)送检样本:石蜡切片
检测项目:甲状腺癌基因检测套餐全?版(28基因突变+33基因融合)
本次受检者经临床病理确诊为甲状腺乳头状癌患者,属于甲状腺癌中常见的亚型,也是预后较好的类型。PTC肿瘤恶性程度较低,患者10年生存率可以达到90%—95%,仅5%左右的患者可能会出现周围淋巴结或肺转移,但经过手术治疗,整体预后相对较好。
RET基因融合,辅助鉴别甲状腺结节良恶性
受检者检出的RET基因融合是导致甲状腺癌(发生率约6%)、非小细胞肺癌(1.4%—2.5%)等多种癌症的重要因素。在融合发生机制上,RET基因断裂与其他基因接合的方式发生重组,形成一个含有RET基因C端与另一基因N端的新的融合基因。由于伴侣基因失去泛素化降解,使RET基因酪氨酸活化结构域变构,暴露磷酸化位点引起RET蛋白活化,从而增强信号转导功能,导致肿瘤发生。
据统计,约10%~20%的PTC患者存在RET基因融合变异。《甲状腺结节和分化型甲状腺癌诊治指南》明确,与BRAF基因一样,RET基因融合也能够为甲状腺结节的良恶性提供指导,通过NGS多基因检测会有利于提高诊断的灵敏度,同时强调甲状腺分子病理报告中需要包括BRAF、RAS、TERT等基因突变及RET融合变异情况。因此,RET融合的检测不仅限于晚期的甲状腺癌患者,在甲状腺结节良恶性鉴别时就有必要,以辅助明确甲状腺结节的良恶性,并评估恶性甲状腺结节的预后和靶向治疗。
PTC患者是预后较好的甲状腺癌亚型,这一结论非空穴来风。在甲状腺癌指南中提到,多数PTC呈惰性经过且预后良好,与PTC相关的独立危险因素包括年龄、肿瘤大小、分期、甲状腺外侵犯以及远处转移。指南还细分了PTC不同组织学亚型分子病理诊断和预后评估,BRAF/RET/NRAS/TERT/PIK3CA/TP53/ALK/CTNNB1等多个基因变异为PTC的亚型确认、预后评估和临床诊治提供了指导。
去年,Ann Surg Oncol上发表回顾性研究,纳入的327例PTC手术后患者中,14(4.3%)例检出RET融合变异,相比RET野生型且BRAF突变(RET-/BRAF+)或RAS突变(RET-/RAS+)患者,携带RET融合的肿瘤展现出更高的侵袭性,表现为更高的外部浸润率(50% vs 27% vs 2.2%),更高频率的多病灶(85.7% vs 60.3% vs 44.4%),更高频率的远处转移率(14.3% vs 1.1% vs 0%)以及更差的生存率。
在《甲状腺癌RET基因检测与临床应用专家共识》中明确建议,伴有RET基因重排/融合的PTC恶性程度更高,建议尽早积极外科手术治疗。而且CCDC6-RET(本案例患者检出)和NCOA4-RET是最为常见的融合形式,经ARROW临床研究证实占比分别为55%和18%。
因此,即便甲状腺乳头状癌预后相对较好,就RET融合甲状腺癌的特征而言,仍需要更积极的外科治疗和后续靶向治疗。现阶段,不仅是甲状腺癌,对于RET融合变异的实体瘤患者来说,靶向药物的陆续获批着实为他们点燃了希望!
RET基因融合,指导甲状腺癌患者靶向药物治疗
目前,NMPA已经批准普拉替尼(普吉华)和塞普替尼(妥睿)两款靶向药物,用于治疗晚期或转移性RET融合阳性的甲状腺癌患者,实现了RET融合甲状腺癌患者国内靶向药的可及。那么疗效如何呢?我们参考官方研究数据。
普拉替尼治疗晚期经卡博替尼和/或凡德他尼治疗的RET融合阳性甲状腺癌患者,是基于ARROW临床试验结果[7],研究纳入了8例RET融合的甲状腺癌,客观缓解率(ORR)达到89%,疾病控制率(DCR)为100%,且耐受性良好。
塞普替尼获批治疗晚期接受过系统治疗的RET融合阳性的甲状腺癌患者,是基于LIBRETTO-001临床试验,纳入22例经治的RET融合阳性甲状腺癌患者中,中位随访时间为20.27个月,ORR为77.3%,临床获益率为100.0%,中位DOR为18.4个月,1年无进展生存率为68.6%。而且,12例未经治疗的RET融合甲状腺癌患者中,ORR也高达92%。证实无论是系统治疗后,还是一线治疗的RET融合甲状腺癌患者,均能从塞普替尼靶向治疗中获益。在后期的LIBRETTO-321研究中,入组的1名RET融合TC初治患者,接受了23.4周治疗,并在第8周疗效评估达到PR,大肿瘤负荷缩小43%,至试验数据截止时,缓解仍在持续。
另外,今年发表在HEAD AND NECK CANCER期刊上的研究总结了甲状腺癌不同通路基因变异的靶向治疗方案和作用机理,除了普拉替尼和塞普替尼之外,包括凡德他尼,卡博替尼,培唑帕尼、舒尼替尼等多靶点抑制剂能为RET基因变异的患者带来获益可能。
甲状腺基因检测,除了RET基因之外,还有多个驱动基因突变受到国内外指南的检测推荐,彰显出甲状腺癌多基因检测的重要意义。今年发表在GENE上的一篇综述Update on Molecular Diagnostics in Thyroid Pathology:A Review中整理了甲状腺癌患者获批的靶向和免疫治疗方案。相信未来有更多以基因突变为指导的靶向药物将获益于甲状腺癌患者。
文章摘自网络,侵删
同类文章排行
- NGS助力甲状腺癌患者检出RET融合,多角度指导临床诊治!
- 提升淋巴瘤患者5年生存率的“三个法宝”
- 疾病控制达85.3%!硼中子治疗脑肿瘤、头颈癌等癌种疗效明显
- 北京积水潭医院MDT团队为卵巢癌患者完成高难度复杂手术
- 顾建英教授团队在黑色素瘤转移机制研究方面获新突破!
- BRAF-MEK抑制剂在新诊断的乳头型颅咽管瘤中的应用
- 针对癌症细胞的精准打击
- 胶质瘤分级有哪些?严重吗?得了胶质瘤能活多久?
- 质子治疗比传统放疗更安全吗?
- 骨侵袭性脑膜瘤罕见吗?骨侵袭性脑膜瘤应该怎么治疗?
最新资讯文章
您的浏览历史








