分散—即时性CAR-T细胞疗法:多发性骨髓瘤领域的“工业变革”?
BCMA嵌合抗原受体(CAR)t细胞疗法代表了多发性骨髓瘤治疗的重大突破。Idecabtagenevicleucel和ciltacabtageneautoleucel是迄今仅有的两种获批的工业BCMACARt细胞疗法。在复发性或难治性多发性骨髓瘤中,两者均显示出前所未有的临床疗效,转化为无进展生存期,大大超过了预期的3~4个月无进展生存期。本期《柳叶刀肿瘤学》(TheLancetOncology)中,AinaOliver-Caldés及其同事在上报告了ARI0002h治疗30例复发性或难治性多发性骨髓瘤患者的结果,ARI0002h是一个学术小组在西班牙开发的BCMACARt细胞疗法。本研究证实,所有30例患者均缓解,在学术环境中按照《药品生产质量管理规范》标准进行内部生产CART细胞是可行的,可以生产出具有强效活性的高质量产品。下面,让我们跟随这支西班牙医疗团队的脚步来见证这场神奇的CAR-T试验吧。
如何简单理解CAR-T疗法的工作原理?
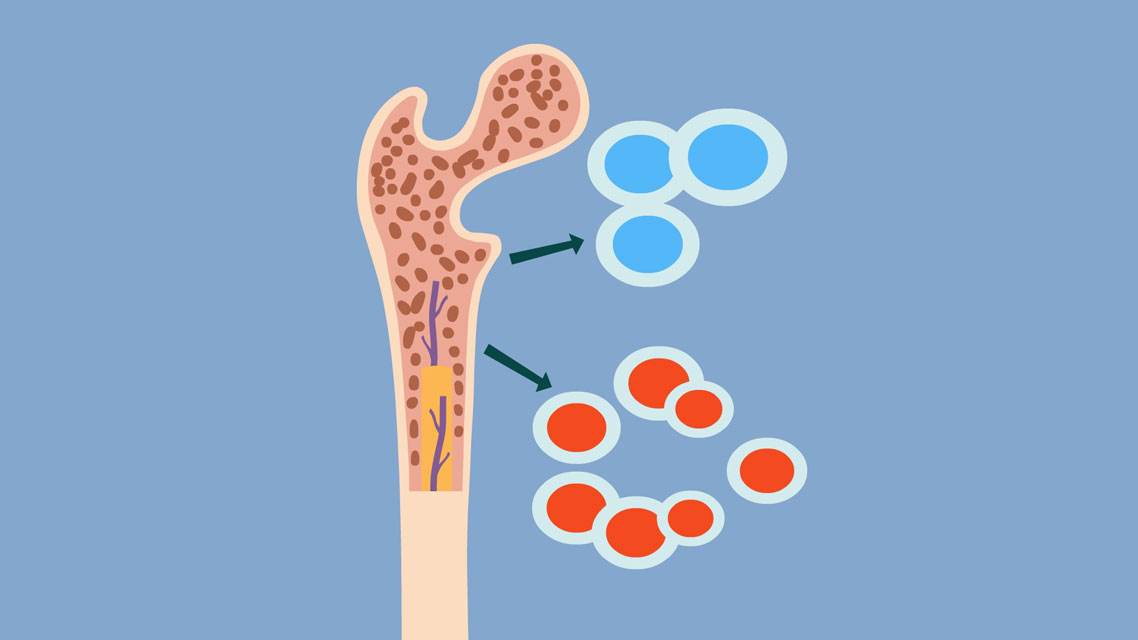
下图是CAR(嵌合抗原受体)T细胞免疫疗法的插图,这是一个正在开发的治疗癌症的过程。T细胞(左上角的一个)是人体免疫系统的一部分,从患者体内提取,其DNA(脱氧核糖核酸)被病毒(紫色)修饰,从而产生嵌合抗原受体(CAR)蛋白。这些蛋白质对病人的癌症有特异性。经过修饰的T细胞在实验室中繁殖,然后被重新引入患者体内。
多发性骨髓瘤的CAR-T疗法的兴起
自2008年以来,由于将蛋白酶体抑制剂、免疫调节剂和抗cd38单克隆抗体联合应用于标准治疗,多发性骨髓瘤患者的生存期得到了改善。尽管如此,仍有很大比例的患者持续复发,多药耐药仍然是导致复发或难治性多发性骨髓瘤患者预后不良的重要挑战。嵌合抗原受体(CAR)t细胞疗法已成为复发性或难治性多发性骨髓瘤的有前景选择。几种靶向BCMA的CARt细胞制品正在临床研究中。然而,只有两种BCMACARt细胞疗法(idecabtagenevicleucel和ciltacabtageneautoleucel)获得了美国食品药品监督管理局(fda)和欧洲药品管理局(ema)的批准,这两种疗法是在之前至少4线疗法和至少3线疗法之后获得的,用于治疗多发性骨髓瘤,包括蛋白酶体抑制剂、免疫调节剂和抗cd38单克隆抗体。
分散即时性CAR-T疗法:ARI0002h
ARI0002h是一种基于人源化4-1bb的BCMA-CART细胞疗法,通过外周血白细胞单采术获得的自体T细胞进行慢病毒转导,已在临床前的体外和体内方法中证明其抗肿瘤活性。西班牙学术机构开发了两种CARt细胞结构;1个靶向CD19(ARI-0001;varnimcabtageneautoleucel)和另一种抗BCMA(ARI0002h)。使用ARI-0001治疗成人和儿童cd19阳性恶性肿瘤的CART19-BE-01多中心临床试验使其于2021年2月在西班牙获得了医院豁免批准,这使其成欧洲临床应用的一种学术性CARt细胞疗法。
CARTBCMA-HCB-01试验过程与结果
试验控制
CARTBCMA-HCB-01是在西班牙5个学术中心进行的一项单组、开放标签研究。患者纳入标准为复发或难治性多发性骨髓瘤;年龄18~75岁;美国东部肿瘤协作组体能状态评分为0~2分;既往接受过两线或两线以上的治疗,包括蛋白酶体抑制剂、免疫调节剂和抗cd38抗体;对后一线治疗无效;根据国际骨髓瘤工作组(IMWG)标准可测量病变(血清和尿单克隆蛋白10g/L或200mg/24h,累及游离轻链100mg/L);预期寿命超过3个月。排除标准包括既往接受过bcma指导的治疗,以及器官系统功能不全(包括估计肾小球滤过率低于50mL/min)。
试验主要结果
在这项使用ARI0002h(西班牙学术机构巴塞罗那医院诊所(HospitalClinicdeBarcelona)正在开发的靶向BCMA的自体CARt细胞制品)开展的单组、多中心研究中,在既往接受过至少两种治疗方案(包括蛋白酶体抑制剂、免疫调节药物)的复发性或难治性多发性骨髓瘤成人患者中,分次给药的ARI0002h和100日后加强给药使患者达到早期、深度和持久缓解。
试验结论
ARI0002h是复发性或难治性多发性骨髓瘤患者的可行治疗方案,其活性和安全性与已批准的CARt细胞产品相当。鉴于美国和欧洲由于缺乏制造能力和报销,患者获得这些治疗的机会有限,因此促进产品真正获得和施用的即时策略至关重要。
多发性骨髓瘤免疫治疗领域的新发现
首先,研究者使用人源化单链可变片段识别BCMA,而不是使用完全动物来源的单链可变片段(小鼠或美洲驼),从而降低了CAR的潜在免疫原性,而已经批准的商业化CART细胞就是这种情况。其次,研究者采用分次给药方案降低了毒性,未观察到神经毒性病例。第三,本试验计划在100日后在达到缓解且无相关毒性的患者中给予第二剂,提供新鲜且有活性的CART细胞,以巩固或加深缓解。最后,本试验纳入了细胞治疗中的即时治疗概念,表明在公共卫生系统中,基于两个生产中心和5家治疗医院的策略是可能的。
分散即时性CAR-T疗法对比传统CAR-T的优势
对CARt细胞疗法的需求正在增加,研究者推测它将被引入更早的治疗线。然而,高成本、制造延迟以及由工业驱动的集中式CARt细胞生产的潜在瓶颈可能限制了该疗法的应用。此外,尽管欧盟委员会批准了idecabtagenevicleucel和ciltacabtageneautoleucel,但由于没有报销协议,这两种产品在西班牙和其他几个欧洲国家无法获得。ARI0002h是一种学术性CARt细胞疗法,已在西班牙的两家机构生产,是这两个中心(巴塞罗那和潘坡纳)真正的即时生产方法。这种方法可以增加可用于生产的插槽数量,允许在患者的临床情况需要时快速释放;在研究者的研究中,这个时间只有19天。ARI0002h的制造成本高达商用CART细胞的1/4。基于这些原因,研究者相信在学术机构生产的CART细胞将成为改善世界各地的可及性的关键。
未来展望与总结
Idecabtagenevicleucel和ciltacabtageneautoleucel由上市许可持有人拥有和运营的大型集中设施生产。然而,与这种集中方法相比,本研究和其他学术研究采用了分散的床旁治疗模式。这种模式规避了与集中制造相关的复杂和耗时的物流,从而降低了成本,缩短了周转时间。不可否认,制药行业推动了CARt细胞领域的发展,使许多患者获得了这种治疗,并使卫生当局相信有必要报销。学术举措(如Oliver-Caldés及其同事的举措)有助于及时探索新的创新概念,并进一步提高这一备受欢迎的疗法的可及性。因此,产业驱动和学术驱动的模式并不相互排斥。合作项目正在兴起,所有这些举措都有一个共同目标:加速和加快CARt细胞的应用,并改善复发性或难治性多发性骨髓瘤患者的结局。
文章源自网络,如有侵权请联系删除
同类文章排行
- 血液科联合发布PVD方案在治疗新诊断伴肾功能损害的多发性骨髓瘤的探索
- NALIRIFOX方案:转移性胰腺导管癌患者的新希望
- JCP:基于CRISPR-Cas9的选择性指数扩增检测晚期胰腺癌患者血浆中KRAS突变的性能评估
- 黑科技T细胞疗法突破性案例:存活超25年,病灶消失,持续缓解
- 新辅助、辅助还是两者兼而有之?NSCLC的争论愈演愈烈
- 孙学军教授团队揭示结直肠癌细胞化疗耐药新机制
- 肿瘤骨转移,唑来膦酸给药间隔或能大幅延长
- 《国际癌症期刊》:癌症发病率增加3倍,艾滋患者如何自我保护?
- 120万一针抗癌?河南接受CAR-T疗法的癌症患者,如今咋样了?
- 一发现就是晚期 生存率极低!胰腺癌为什么这么可怕
最新资讯文章
您的浏览历史